La señal para que comience la pubertad se inicia en el cerebro, concretamente en el hipotálamo. Allí, neuronas especializadas liberan la hormona liberadora de gonadotropinas (GnRH), que activa la hipófisis —en la base del cráneo— para que esta segregue otras hormonas que estimulan la maduración de las gónadas (ovarios en las mujeres y testículos en los hombres). Este proceso, que culmina en la fertilidad, se conoce como el eje hipotálamo-hipófiso-gonadal (HPG).
Hasta ahora se pensaba que esta regulación dependía principalmente de redes neuronales. Sin embargo, un estudio reciente del Centro Nacional de Investigaciones Oncológicas (CNIO) ha revelado dos elementos inesperados en este mecanismo: la microglía —células inmunitarias residentes en el sistema nervioso central— y la proteína RANK (receptor activator of nuclear factor κB), conocida por su rol en la remodelación ósea y el desarrollo de las glándulas mamarias.
La investigación, publicada en la prestigiosa revista Science (12 de marzo de 2026), está liderada por Eva González-Suárez, jefa del Grupo de Transformación y Metástasis del CNIO —quien ya había descubierto en 2010 el papel clave de RANK en el cáncer de mama—. El primer autor es el investigador Alejandro Collado.
Las neuronas GnRH son las principales protagonistas del hipotálamo en el control de la pubertad, el desarrollo gonadal y la fertilidad. Aunque se sabía que otras neuronas las modulan, no se había identificado que células inmunitarias pudieran influir directamente en ellas.
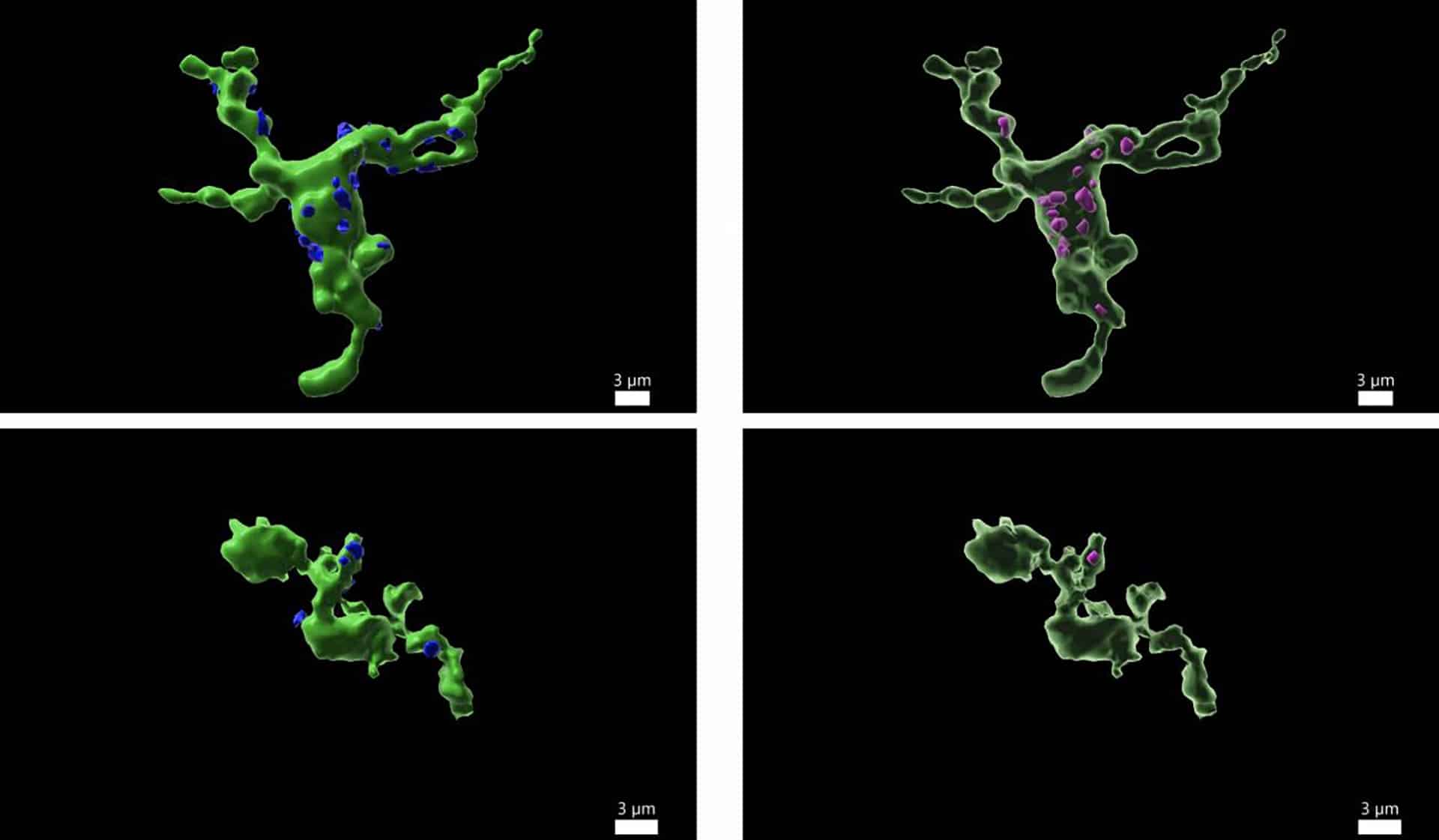
La microglía, encargada de eliminar amenazas y desechos en el cerebro, expresa la proteína RANK y regula así la actividad de las neuronas GnRH. Cuando el equipo suprimió RANK en modelos animales (ratones), se produjeron graves alteraciones reproductivas en ambos sexos.
En animales nacidos sin RANK o en los que se eliminó la proteína antes de la pubertad, se observó una reducción drástica de hormonas sexuales, hipogonadismo hipogonadotrópico (pérdida de función gonadal por falta de estimulación hipofisaria) y ausencia o retraso puberal. En ejemplares adultos sexualmente maduros, la eliminación de RANK provocó infertilidad en apenas un mes.
Estos hallazgos indican que la señalización RANK en la microglía es esencial no solo para iniciar la pubertad, sino también para mantener la fertilidad a lo largo de la vida adulta. La pérdida de RANK altera la activación y morfología de la microglía en la eminencia media del hipotálamo, reduce los contactos entre microglía y proyecciones de neuronas GnRH, y disminuye la respuesta de estas neuronas a señales como la kisspeptina.
Para explorar la relevancia en humanos, el equipo analizó muestras de pacientes con hipogonadismo hipogonadotrópico congénito (HHC), un trastorno raro que causa retraso o ausencia de pubertad e infertilidad, asociado tradicionalmente a defectos en las neuronas GnRH o sus moléculas reguladoras.
En algunos de estos pacientes se identificaron mutaciones raras en el gen que codifica RANK. Esto convierte a RANK en un gen candidato para el diagnóstico molecular del HHC y abre la puerta a considerarlo una posible diana terapéutica para alteraciones endocrinas y síndromes de infertilidad.